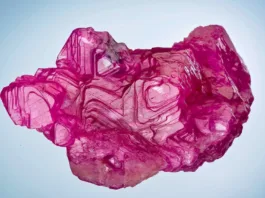
Anatase is een van de drie primaire minerale vormen van titanium dioxide (TiO2), de andere twee zijn rutiel en brookiet. Het is een tetragonaal mineraal en een polymorf van TiO2, wat betekent dat het dezelfde chemische samenstelling heeft als rutiel, maar een andere kristalstructuur heeft. Anatase is vernoemd naar het Griekse woord ‘anatasis’, wat uitbreiding betekent, verwijzend naar de langere kristallen assen vergeleken met die van rutiel.

Chemische samenstelling: De chemische samenstelling van anataas wordt weergegeven door de formule TiO2, wat aangeeft dat het bestaat uit één titanium (Ti) atoom gebonden aan twee zuurstof (O) atomen. Deze samenstelling is hetzelfde als die van rutiel, maar de rangschikking van de atomen binnen het kristalrooster verschilt, wat leidt tot verschillende fysische eigenschappen.
Kristal structuur: Anatase heeft een tetragonale kristalstructuur, wat betekent dat de eenheidscel vier zijden heeft en groter dan breed is. Het kristalrooster van anataas wordt gekenmerkt door een vervormde octaëdrische coördinatiegeometrie rond elk titaniumatoom. In eenvoudige bewoordingen zijn de titaniumatomen omgeven door zes zuurstofatomen, die een octaëdrische vorm vormen. De tetragonale structuur van anataas staat in contrast met de rutielpolymorf, die een compactere, orthorhombische kristalstructuur heeft.
De kristalstructuur beïnvloedt de eigenschappen van anataas, waardoor het bij verschillende toepassingen ander gedrag vertoont dan rutiel. Anatase staat bekend om zijn fotokatalytische eigenschappen, die toepassing vinden in milieu- en energiegerelateerde processen. Het heeft een hogere oppervlaktereactiviteit dan rutiel, waardoor het bruikbaar is in fotokatalyse, zonnecellen en andere technologieën.
Samenvattend is anataas een minerale vorm van titaniumdioxide met een tetragonale kristalstructuur, verschillend van de rutiel- en brookietpolymorfen. De unieke eigenschappen maken het waardevol in verschillende technologische toepassingen, vooral op gebieden die verband houden met fotokatalyse en zonne-energie.
Inhoud
Eigenschappen van Anatase

Fysieke eigenschappen
- Kleur: Anatase is meestal donkerblauw, bruin of zwart, maar kan ook verschijnen in de kleuren geel, groen of rood. De kleur kan variëren als gevolg van onzuiverheden in het kristalrooster.
- Glans: Het mineraal heeft een submetallische tot metaalachtige glans, waardoor het een glanzend uiterlijk krijgt wanneer licht op het oppervlak reflecteert.
- Streep: De streep anataas is wit tot lichtgeel, wat de kleur is van het poedervormige mineraal wanneer het over een streepplaat wordt geschraapt.
- Hardheid: Anatase heeft een Mohs-hardheid van 5.5–6, waardoor het een matig hard mineraal is. Het kan glas krassen, maar is zachter dan mineralen als kwarts.
- Dichtheid: De dichtheid van anataas varieert, maar ligt over het algemeen rond 3.8 tot 3.9 g/cm³.
- Inkijk: Anatase vertoont een slechte of onduidelijke splitsing, wat betekent dat het niet langs gladde vlakken breekt wanneer het wordt blootgesteld aan spanning.
- Transparantie: Het mineraal is doorgaans ondoorzichtig, wat betekent dat er geen licht doorheen gaat.
- Kristallijn systeem: Anataas kristalliseert in het tetragonale systeem en vormt kristallen met vier zijden, die vaak voorkomen als prisma's of tabelvormige kristallen.
Chemische eigenschappen:
- Chemische formule: TiO2 – Anatase heeft dezelfde chemische formule als rutiel en brookiet, allemaal verschillende polymorfen van titaniumdioxide.
- Reactiviteit: Anatase staat bekend om zijn hogere reactiviteit in vergelijking met rutiel. Het vertoont aanzienlijke fotokatalytische activiteit, waardoor het bruikbaar is in toepassingen zoals milieusanering en conversie van zonne-energie.
- Fotokatalytische eigenschappen: Een van de opmerkelijke chemische eigenschappen van anataas is het vermogen om fotokatalyse te ondergaan. Bij blootstelling aan ultraviolet licht kan anatase verschillende chemische reacties katalyseren, zoals de afbraak van organische verontreinigende stoffen in water.
- Transformatie naar rutiel: Bij verhoogde temperaturen kan anataas een fasetransformatie naar rutiel ondergaan. Deze transformatie is een omkeerbaar proces en wordt beïnvloed door factoren zoals temperatuur en druk.
- Thermische stabiliteit: Anatase is over het algemeen minder thermisch stabiel dan rutiel, en de stabiliteit ervan wordt beïnvloed door omstandigheden zoals druk en de aanwezigheid van onzuiverheden.
Het begrijpen van zowel de fysische als de chemische eigenschappen van anataas is cruciaal voor het gebruik ervan in verschillende industriële toepassingen, waaronder fotokatalyse, pigmenten en als onderdeel bij de productie van titaniumdioxide voor verven, coatings en andere producten.
Optische eigenschappen van Anatase
- Transparantie:
- Anatase is doorgaans ondoorzichtig, wat betekent dat er geen licht doorheen gaat. Dit in tegenstelling tot mineralen die transparant of doorschijnend zijn.
- Breking:
- De brekingsindex van anataas is relatief hoog, wat bijdraagt aan de karakteristieke glans. De brekingsindex is een maatstaf voor hoeveel licht wordt gebogen of gebroken wanneer het door het mineraal gaat.
- dubbele breking:
- Anatase vertoont dubbele breking, een eigenschap waarbij licht in twee stralen wordt gesplitst terwijl het door het mineraal gaat. De mate van dubbele breking wordt beïnvloed door de kristalstructuur en oriëntatie.
- Spreiding:
- Dispersie verwijst naar de scheiding van verschillende kleuren licht terwijl het door een materiaal gaat. Anatase kan enige spreiding vertonen, wat bijdraagt aan het kleurenspel, maar deze is niet zo uitgesproken als bij sommige andere mineralen.
- Pleochroïsme:
- Anatase kan pleochroïsme vertonen, wat betekent dat het verschillende kleuren vertoont wanneer het vanuit verschillende hoeken wordt bekeken. De aanwezigheid van pleochroïsme houdt vaak verband met de oriëntatie van kristallen assen.
- Optische klasse:
- Anatase behoort tot het tetragonale kristalsysteem en de optische klasse is uniaxiaal positief. Dit betekent dat het één optische as heeft en dat licht dat langs deze as reist positieve dubbele breking ervaart.
- Glans:
- Het mineraal heeft een submetaalachtige tot metaalachtige glans, wat bijdraagt aan de glans bij blootstelling aan licht.
- fluorescentie:
- Anatase kan fluorescentie vertonen onder ultraviolet (UV) licht, met kleurvariaties afhankelijk van de aanwezigheid van specifieke onzuiverheden.
Het begrijpen van de optische eigenschappen van anataas is belangrijk voor zowel geologische als industriële doeleinden. Deze eigenschappen kunnen worden gebruikt bij de identificatie van het mineraal in geologische monsters en kunnen ook de toepassingen ervan in verschillende industrieën beïnvloeden, waaronder pigmenten, coatings en optische apparaten.
Voorkomen en vorming

Voorval:
Anatase is een mineraal dat in verschillende geologische omgevingen voorkomt. Het wordt vaak aangetroffen in combinatie met andere titaniummineralen, met name rutiel en brookiet. Enkele veelvoorkomende gebeurtenissen zijn:
- Pegmatieten: Anatase is te vinden in pegmatiet aderen, die grofkorrelig zijn stollingsgesteenten. Pegmatieten bevatten vaak een verscheidenheid aan mineralen vanwege hun langzame afkoeling en de aanwezigheid van vluchtige componenten tijdens hun vorming.
- Metamorfe gesteenten: Anatase wordt soms in metamorfose aangetroffen rotsen, vooral die welke hoge temperaturen en hoge druk hebben ondergaan. Voorbeelden hiervan zijn schisten en gneis.
- Hydrothermische aderen: Hydrothermale aderen, gevormd door de afzetting van mineralen uit hete, mineraalrijke vloeistoffen, kunnen ook anataas bevatten. Deze aderen komen veel voor in een reeks geologische omgevingen.
- Plaats Deposito: Anatase kan, samen met andere zware mineralen, geconcentreerd worden in placerafzettingen door het proces van erosie, transport en sedimentatie. Deze afzettingen worden vaak geassocieerd met riviersystemen.
- Sedimentair gesteente: Anatase kan voorkomen in sedimentair gesteente, waaronder zandsteen en schalie. Het kan aanwezig zijn als afvalkorrels of als onderdeel van het cementeermateriaal.
Opleidingen:
Bij de vorming van anataas zijn processen betrokken leiden tot de kristallisatie van titaniumdioxide onder specifieke omstandigheden. De exacte mechanismen kunnen variëren afhankelijk van de geologische omgeving, maar veel voorkomende vormingsprocessen zijn onder meer:
- Magmatische processen: Anatase kan kristalliseren uit magmatische vloeistoffen tijdens het afkoelen van magma. Terwijl het magma afkoelt, kunnen mineralen zoals anataas, rutiel en brookiet neerslaan.
- Hydrothermische processen: Hete, mineraalrijke vloeistoffen die in de aardkorst circuleren, kunnen leiden tot de vorming van anataas. Deze vloeistoffen kunnen titanium uit omringende rotsen oplossen en vervolgens anataas afzetten terwijl ze afkoelen.
- Metamorfose: Anatase kan zich vormen tijdens metamorfose, waarbij de wijziging van gesteenten als gevolg van hoge temperatuur en druk. In metamorfe gesteenten kunnen de voorlopermineralen veranderingen ondergaan om anataas te worden.
- Verwering en erosie: Anatase kan door verweringsprocessen uit de oorspronkelijke brongesteenten worden bevrijd. Eenmaal vrijgekomen, kan het door water en wind worden getransporteerd en zich uiteindelijk ophopen in sedimentaire omgevingen.
Het begrijpen van het voorkomen en de vorming van anataas is cruciaal voor zowel geologische studies als industriële toepassingen. De aanwezigheid van het mineraal in bepaalde geologische omgevingen kan inzicht verschaffen in de geschiedenis en processen van de aarde, terwijl zijn eigenschappen het waardevol maken voor verschillende technologische toepassingen.
Toepassingen en gebruik van Anatase

Anatase vindt vanwege zijn unieke fysische en chemische eigenschappen toepassingen op verschillende industriële en technologische gebieden. Enkele van de opmerkelijke toepassingen van anatase zijn onder meer:
- Fotokatalyse: Anatase staat bekend om zijn fotokatalytische activiteit. Bij blootstelling aan ultraviolet (UV) licht kan het chemische reacties katalyseren, zoals de afbraak van organische verontreinigende stoffen in lucht en water. Deze eigenschap wordt gebruikt in milieutoepassingen, waaronder waterzuivering en luchtbehandeling.
- Zonnepanelen: De halfgeleidereigenschappen van anataas maken het geschikt voor gebruik in zonnecellen. Het kan worden gebruikt als fotoanodemateriaal in kleurstofgevoelige zonnecellen (DSSC's) en als onderdeel van de fotoactieve laag in andere soorten zonneceltechnologieën. Het vermogen om UV-licht te absorberen sluit goed aan bij het zonnespectrum.
- Pigmenten en kleurstoffen: Anatase wordt gebruikt bij de productie van pigmenten en kleurstoffen voor verven, coatings en kunststoffen. De unieke kleuren en optische eigenschappen maken het waardevol bij het creëren van een reeks tinten in verschillende materialen.
- katalyse: Anatase wordt gebruikt als katalysator bij chemische reacties. De oppervlaktereactiviteit ervan is voordelig bij het bevorderen van bepaalde chemische transformaties, en vindt toepassingen in de synthese van organische verbindingen en andere industriële processen.
- cosmetica: Anatase wordt gebruikt in cosmetische producten, waaronder zonnebrandmiddelen en huidverzorgingsproducten. De UV-absorberende eigenschappen maken het effectief in het beschermen van de huid tegen schadelijke UV-straling.
- keramiek: Anatase wordt in keramiek verwerkt om de eigenschappen ervan te verbeteren. Het kan de mechanische sterkte en thermische stabiliteit van keramische materialen verbeteren.
- Optische apparaten: De optische eigenschappen van anataas, waaronder de hoge brekingsindex en dubbele breking, maken het geschikt voor gebruik in optische apparaten zoals lenzen en prisma's.
- Bouwmaterialen: Anatase kan worden toegevoegd aan bouwmaterialen, zoals beton en coatings, om bepaalde wenselijke eigenschappen te verlenen. De fotokatalytische activiteit kan bijdragen aan de zelfreinigende en luchtzuiverende eigenschappen van deze materialen.
- Watersplitsing: Bij onderzoek en ontwikkeling voor toepassingen op het gebied van hernieuwbare energie wordt anataas onderzocht op zijn potentiële gebruik bij watersplitsingsreacties. Bij dit proces wordt zonne-energie gebruikt om water te splitsen in waterstof en zuurstof, die kunnen worden gebruikt als schone en duurzame brandstofbron.
De diverse toepassingen van anataas benadrukken het belang ervan in verschillende technologische ontwikkelingen, van milieusanering tot energieproductie en materiaalkunde. Lopend onderzoek blijft nieuwe manieren verkennen om de unieke eigenschappen van anataas te benutten voor opkomende technologieën.
Vergelijking met andere titaandioxidepolymorfen
Titaandioxide (TiO2) bestaat in verschillende polymorfe vormen, waarbij de drie belangrijkste vormen rutiel, anataas en brookiet zijn. Hier is een vergelijking tussen anataas en de andere twee grote polymorfen:

1. Anatase versus Rutiel:
- Kristal structuur:
- Anatase: Tetragonale kristalstructuur.
- Rutiel: Orthorhombische kristalstructuur.
- Kleur:
- Anatase: Gevarieerde kleuren, waaronder blauw, bruin, zwart, geel, groen en rood.
- Rutiel: Roodbruin tot zwart.
- Optische eigenschappen:
- Anatase: Hogere brekingsindex, vertoont dubbele breking en pleochroïsme.
- Rutiel: Lagere brekingsindex, niet dubbelbrekend.
- Fotokatalytische activiteit:
- Anatase: Hogere fotokatalytische activiteit, vooral onder UV-licht.
- Rutiel: Lagere fotokatalytische activiteit maar stabieler onder zichtbaar licht.

Kharan, Kharan-district, Balochistan (Baluchistan), Pakistan
2. Anatase versus Brookite:
- Kristal structuur:
- Anatase: Tetragonale kristalstructuur.
- Brookiet: Orthorhombische kristalstructuur.
- Kleur:
- Anatase: Gevarieerde kleuren.
- Brookiet: Bruin tot zwart, soms met een rode tint.
- Voorval:
- Anatase: Vaker voorkomend en stabiel bij lagere temperaturen.
- Brookiet: Minder vaak voorkomend en stabiel bij hogere temperaturen.
- Optische eigenschappen:
- Anatase: Vertoont dubbele breking en pleochroïsme.
- Brookiet: Vertoont dubbele breking.
Algemene vergelijkingen:
- Fotokatalytische activiteit:
- Anatase: Bekend om hoge fotokatalytische activiteit, vooral in milieutoepassingen.
- Rutiel en Brookiet: Lagere fotokatalytische activiteit vergeleken met anataas.
- Stabiliteit:
- Anatase: Minder stabiel dan rutiel bij hoge temperaturen.
- Rutiel: Thermisch stabieler.
- Brookiet: Minder stabiel dan anataas maar stabieler dan anataas bij hoge temperaturen.
- toepassingen:
- Anatase: Op grote schaal gebruikt in fotokatalyse, zonnecellen, pigmenten en cosmetica.
- Rutiel: Gebruikt in pigmenten, coatings, kunststoffen en sommige optische toepassingen.
- Brookiet: Minder gebruikelijk in toepassingen, maar is onderzocht vanwege zijn unieke eigenschappen.
Samenvattend zijn anataas, rutiel en brookiet verschillende polymorfen van titaniumdioxide, elk met zijn eigen kristalstructuur, kleur, stabiliteit en eigenschappen. Anatase staat vooral bekend om zijn fotokatalytische activiteit, terwijl rutiel wordt gewaardeerd om zijn stabiliteit en de betere prestaties van rutiel onder zichtbaar licht. Brookiet, hoewel minder gebruikelijk, heeft unieke eigenschappen die het voor bepaalde toepassingen interessant maken. De keuze voor de polymorf is afhankelijk van de specifieke eisen van de beoogde toepassing.
Synthese en productie

De synthese en productie van anataastitaandioxide (TiO2) kan via verschillende methoden worden bereikt, waarbij de keuze van de methode vaak afhangt van de gewenste toepassing en de vereiste eigenschappen. Hier zijn enkele veelgebruikte methoden voor de synthese van anataas TiO2:
- Hydrothermische synthese:
- Bij hydrothermische synthese reageren titaniumvoorloperverbindingen met water bij verhoogde temperaturen en drukken. Deze methode kan goed gedefinieerde anataas-nanodeeltjes produceren met gecontroleerde grootte en morfologie. De reactieomstandigheden, zoals temperatuur en druk, kunnen worden aangepast om de kristalstructuur te beïnvloeden.
- Sol-Gel-methode:
- Het sol-gelproces omvat de hydrolyse en polycondensatie van metaalalkoxiden om een sol te vormen, die vervolgens wordt onderworpen aan gelering en drogen. Door de reactieomstandigheden, zoals pH en temperatuur, te controleren, kunnen anataas TiO2-nanodeeltjes worden gesynthetiseerd. De sol-gel-methode maakt de bereiding van dunne films, coatings en andere materialen mogelijk.
- Solvothermische synthese:
- Solvothermische synthese is vergelijkbaar met hydrothermische synthese, maar wordt uitgevoerd in organische oplosmiddelen in plaats van water. Deze methode maakt de synthese van anataas-nanodeeltjes met gecontroleerde grootte en vorm mogelijk. De keuze van het oplosmiddel en de reactieomstandigheden beïnvloeden de eigenschappen van het resulterende TiO2.
- Verbrandingssynthese:
- Verbrandingssynthese omvat de exotherme reactie tussen metaalvoorlopers en een brandstofbron, wat leidt tot de vorming van TiO2-nanodeeltjes. Deze methode is relatief eenvoudig en kosteneffectief, maar vereist mogelijk een zorgvuldige controle van de verbrandingsomstandigheden om de gewenste fase te verkrijgen.
- Chemische dampafzetting (CVD):
- CVD omvat de chemische reactie van gasvormige precursoren om een dunne film TiO2 op een substraat af te zetten. Door de depositieparameters, zoals temperatuur en precursorconcentratie, te controleren, kunnen anataas-TiO2-films worden geproduceerd. CVD wordt vaak gebruikt voor grootschalige productie en in de halfgeleiderindustrie.
- Aerosolmethoden:
- Aerosolmethoden, zoals sproeipyrolyse of vlamsproeipyrolyse, omvatten het genereren van TiO2-nanodeeltjes in de gasfase, die vervolgens op een substraat worden verzameld. Deze methoden zijn geschikt voor het produceren van dunne films en coatings.
- Sjabloonondersteunde methoden:
- Bij template-ondersteunde methoden wordt gebruik gemaakt van templates, zoals micellen van oppervlakteactieve stoffen of nanodeeltjes, om de grootte en structuur van het gesynthetiseerde TiO2 te controleren. Na de synthese wordt het sjabloon verwijderd, waardoor anataas TiO2 met een gedefinieerde structuur achterblijft.
- Mechanische methoden:
- Mechanische methoden, zoals kogelmalen of attritiemalen, omvatten het mechanisch malen of malen van TiO2-voorlopers om fijne deeltjes te verkrijgen. Deze methoden zijn relatief eenvoudig en kunnen worden gebruikt voor grootschalige productie.
De keuze van de synthesemethode hangt af van factoren zoals de gewenste deeltjesgrootte, morfologie en de beoogde toepassing van de anataas TiO2. Elke methode heeft zijn voordelen en beperkingen, en onderzoekers en fabrikanten selecteren vaak de meest geschikte aanpak op basis van specifieke vereisten.